Acid lớp 8: Khái niệm, tính chất, ứng dụng và ví dụ minh họa
Bài 8 KHTN lớp 8 giúp học sinh nhận biết acid, hiểu tính chất hóa học cơ bản, các ứng dụng thực tế và phân biệt acid mạnh – yếu thông qua thí nghiệm và thang pH.
📘 Mục lục bài học
🔹 1. Khái niệm về acid
Acid là hợp chất khi tan trong nước phân ly ra ion H+.
Ví dụ: HCl (axít clohidric), H2SO4 (axít sunfuric), CH3COOH (axít axetic)…
🔹 2. Một số acid thường gặp
- HCl: Axít clohidric – có trong dạ dày, dùng trong công nghiệp làm sạch kim loại.
- H2SO4: Axít sunfuric – cực kỳ mạnh, ăn mòn, có trong ắc quy.
- CH3COOH: Axít axetic – có trong giấm ăn.
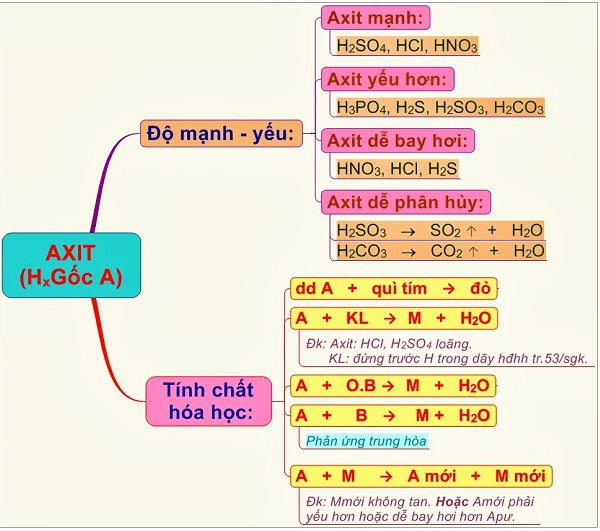
🔹 3. Tính chất hóa học của acid
Acid có 3 tính chất hóa học cơ bản:
- Tác dụng với quỳ tím: Làm quỳ tím chuyển thành màu đỏ.
- Tác dụng với kim loại: Giải phóng khí H2 (trừ kim loại sau H trong dãy hoạt động hóa học).
Ví dụ: Zn + 2HCl → ZnCl2 + H2↑ - Tác dụng với bazơ: Tạo muối và nước (phản ứng trung hòa).
Ví dụ: HCl + NaOH → NaCl + H2O
🔹 4. Ứng dụng thực tế của acid
- HCl: Dùng trong công nghiệp luyện kim, làm sạch bề mặt kim loại.
- H2SO4: Sản xuất phân bón, thuốc nhuộm, ắc quy.
- CH3COOH: Dùng trong thực phẩm, bảo quản và chế biến.
🔹 5. Ví dụ minh họa và thí nghiệm
- Thí nghiệm 1: Nhỏ HCl vào quỳ tím → giấy quỳ chuyển đỏ.
- Thí nghiệm 2: Cho Zn vào dung dịch HCl → có khí H2 thoát ra (nổi bong bóng).
- Thí nghiệm 3: Trộn HCl và NaOH theo tỉ lệ vừa đủ → dung dịch trung hòa, không làm đổi màu quỳ tím.
🔹 6. Ghi nhớ trọng tâm & hướng dẫn học tốt
Kiến thức cần nhớ:
- Acid phân ly ra ion H+ khi tan trong nước.
- Acid làm quỳ tím đổi màu, phản ứng với kim loại và bazơ.
- Nhớ 3 phản ứng hóa học điển hình của acid.
Gợi ý học tốt:
- Học bảng các acid thường gặp và công thức hóa học của chúng.
- Thực hành thí nghiệm hoặc xem video mô phỏng để ghi nhớ tính chất.
- Làm bài trắc nghiệm luyện tập tại hocnhanhstem.com/practice.
- Tham gia mini game tương tác hóa học tại hocnhanhstem.com/game.
👉 Truy cập hocnhanhstem.com để học nhanh – luyện chắc – ghi nhớ sâu kiến thức về acid lớp 8!