Bài Tập Kim Loại Tác Dụng Với Dung Dịch Muối Lớp 9 (Lý Thuyết + Bài Tập)
- A. Lý thuyết
- B. Phương pháp giải
- C. Ví dụ minh họa
- D. Ghi nhớ nhanh
- E. Bài tập tự luyện
- F. 20 câu hỏi trắc nghiệm
- G. 5 câu hỏi đáp
- H. Sơ đồ tư duy minh họa
🔹 Lý thuyết
Phản ứng giữa kim loại và dung dịch muối xảy ra khi kim loại mạnh hơn đẩy kim loại yếu ra khỏi muối:
Phản ứng tổng quát: M1 + M2X → M1X + M2
Trong đó M1 là kim loại đứng trước M2 trong dãy hoạt động hóa học.
Điều kiện phản ứng: Kim loại phản ứng phải đứng trước kim loại trong muối.
🔹 Phương pháp giải
- Tính số mol của các chất đã cho.
- Viết phương trình phản ứng.
- Xác định chất phản ứng hết – dư.
- Tính khối lượng, thể tích sản phẩm theo yêu cầu.
🔹 Ví dụ minh họa
Ví dụ 1: Cho 3,25g Zn vào dung dịch chứa 5,4g CuSO₄. Tính khối lượng kim loại Cu thu được.
Giải:
- PTHH: Zn + CuSO₄ → ZnSO₄ + Cu
- nZn = 3,25/65 = 0,05 mol; nCuSO₄ = 5,4/159 = 0,034 mol
- Cu tạo thành = 0,034 mol → mCu = 0,034 × 64 = 2,176g
🔹 Ghi nhớ nhanh
- Chỉ kim loại mạnh hơn mới đẩy kim loại yếu ra khỏi muối.
- Kim loại không phản ứng với muối của chính nó.
- Sử dụng dãy hoạt động hóa học để so sánh.
🔹 Bài tập tự luyện
- Cho Fe vào dung dịch CuSO₄, tính lượng Cu tạo thành nếu dùng 5,6g Fe.
Hướng dẫn:
nFe = 5,6 / 56 = 0,1 mol
PTHH: Fe + CuSO₄ → FeSO₄ + Cu (1:1)
⟹ nCu = 0,1 mol → mCu = 0,1 × 64 = 6,4g - Cho 3,9g K vào 100ml dung dịch AgNO₃ 0,1M, viết PTHH và tính lượng Ag tạo thành.
Hướng dẫn:
nK = 3,9 / 39 = 0,1 mol; nAg⁺ = 0,1 × 0,1 = 0,01 mol
PTHH: 2K + 2AgNO₃ → 2KNO₃ + 2Ag
Theo PTHH: nAg = 0,01 mol → mAg = 0,01 × 108 = 1,08g - Cho 6,5g Zn vào dung dịch CuSO₄ dư. Tính khối lượng Cu thu được.
Hướng dẫn:
nZn = 6,5 / 65 = 0,1 mol
PTHH: Zn + CuSO₄ → ZnSO₄ + Cu
⟹ nCu = 0,1 mol → mCu = 0,1 × 64 = 6,4g - Cho 10g Al vào dung dịch FeCl₃ dư. Tính khối lượng Fe tạo thành.
Hướng dẫn:
nAl = 10 / 27 ≈ 0,370 mol
PTHH: 2Al + 3FeCl₃ → 2AlCl₃ + 3Fe
⟹ nFe = 0,370 × 3 / 2 ≈ 0,555 mol → mFe ≈ 0,555 × 56 ≈ 31,08g - Cho 13g Mg vào 200ml dung dịch AgNO₃ 0,5M. Tính khối lượng Ag thu được.
Hướng dẫn:
nMg = 13 / 24 = 0,542 mol; nAg⁺ = 0,2 × 0,5 = 0,1 mol
PTHH: Mg + 2AgNO₃ → Mg(NO₃)₂ + 2Ag
⟹ nAg = 0,1 mol → mAg = 0,1 × 108 = 10,8g - Cho 11,2g Fe tác dụng với dung dịch CuSO₄ dư. Tính mCu thu được.
Hướng dẫn:
nFe = 11,2 / 56 = 0,2 mol → mCu = 0,2 × 64 = 12,8g - Cho 7,8g Zn tác dụng với dung dịch Pb(NO₃)₂ dư. Tính lượng Pb tạo ra.
Hướng dẫn:
nZn = 7,8 / 65 = 0,12 mol
PTHH: Zn + Pb(NO₃)₂ → Zn(NO₃)₂ + Pb
⟹ mPb = 0,12 × 207 = 24,84g - Cho 2,7g Al vào dung dịch CuCl₂ dư. Tính khối lượng Cu thu được.
Hướng dẫn:
nAl = 2,7 / 27 = 0,1 mol
PTHH: 2Al + 3CuCl₂ → 2AlCl₃ + 3Cu
⟹ nCu = 0,1 × 3 / 2 = 0,15 mol → mCu = 0,15 × 64 = 9,6g - Cho 4,05g Fe vào 200ml dung dịch AgNO₃ 0,2M. Tính mAg tạo ra.
Hướng dẫn:
nFe = 4,05 / 56 ≈ 0,072 mol; nAg⁺ = 0,2 × 0,2 = 0,04 mol
PTHH: Fe + 2AgNO₃ → Fe(NO₃)₂ + 2Ag
⟹ nAg = 0,04 mol → mAg = 0,04 × 108 = 4,32g - Cho 5,4g Al vào 250ml dung dịch FeCl₃ 0,2M. Tính mFe tạo thành.
Hướng dẫn:
nAl = 5,4 / 27 = 0,2 mol; nFe³⁺ = 0,25 × 0,2 = 0,05 mol
PTHH: 2Al + 3FeCl₃ → 2AlCl₃ + 3Fe
Tỉ lệ: nFe = 0,05 mol → mFe = 0,05 × 56 = 2,8g
🔹 20 Câu Hỏi Trắc Nghiệm (Có Đáp Án & Giải Thích)
- Kim loại nào sau đây phản ứng được với dung dịch CuSO₄?
A. Ag B. Fe C. Au D. Hg
Giải thích: Fe đứng trước Cu trong dãy hoạt động hóa học nên có thể đẩy Cu ra khỏi dung dịch muối CuSO₄. - Cho Mg vào dung dịch ZnSO₄, hiện tượng xảy ra là:
A. Không phản ứng B. Có khí bay lên C. Zn kết tủa D. Dung dịch sôi
Giải thích: Mg hoạt động mạnh hơn Zn nên đẩy Zn ra khỏi muối, tạo kết tủa Zn. - Kim loại nào không đẩy được Cu ra khỏi dung dịch CuSO₄?
A. Ag B. Fe C. Zn D. Al
Giải thích: Ag đứng sau Cu trong dãy hoạt động hóa học nên không phản ứng với CuSO₄. - Cho 1,3g Zn vào 100ml dung dịch CuSO₄ 0,1M. Khối lượng Cu thu được là:
A. 0,64g B. 0,32g C. 0,8g D. 0,16g
Giải thích: Tính mol Zn và Cu²⁺, Zn dư → tính khối lượng Cu từ 0,001 mol Cu²⁺. - Kim loại nào sau đây phản ứng được với dung dịch AgNO₃?
A. Cu B. Zn C. Pb D. Au
Giải thích: Zn hoạt động mạnh hơn Ag nên đẩy Ag ra khỏi dung dịch muối. - Trong phản ứng Fe + CuSO₄ → FeSO₄ + Cu, kim loại bị đẩy ra là:
A. Cu B. Fe C. Zn D. Mg
Giải thích: Cu là kim loại trong muối bị đẩy ra do Fe mạnh hơn. - Hiện tượng khi cho dây sắt vào dung dịch CuSO₄:
A. Dây sắt tan dần B. Dung dịch có màu xanh C. Xuất hiện lớp đỏ bám vào sắt D. Không có hiện tượng
Giải thích: Cu kết tủa màu đỏ bám vào sắt, sắt tan ra tạo muối Fe²⁺. - Phản ứng giữa kim loại và dung dịch muối là phản ứng:
A. Thế B. Oxi hóa C. Nhiệt phân D. Thế – Oxi hóa khử
Giải thích: Phản ứng xảy ra kèm sự trao đổi electron (oxi hóa khử). - Cho Mg dư vào dung dịch Cu(NO₃)₂, sau phản ứng dung dịch thu được là:
A. Mg(NO₃)₂ B. Mg(NO₃)₂ và Cu C. Cu(NO₃)₂ D. Mg
Giải thích: Mg phản ứng tạo muối mới Mg(NO₃)₂ và đẩy Cu ra khỏi dung dịch. - Kim loại Fe phản ứng được với dung dịch muối nào sau đây?
A. NaCl B. CuSO₄ C. ZnSO₄ D. FeCl₃
Giải thích: Chỉ muối của kim loại yếu hơn Fe mới phản ứng (Cu). - Khi Fe dư vào dung dịch AgNO₃ dư, sản phẩm thu được là:
A. FeNO₃ và Ag B. Fe(NO₃)₃ và Ag C. Fe₂O₃ D. Ag₂SO₄
Giải thích: Fe bị oxi hóa thành Fe³⁺, tạo muối sắt (III), Ag kết tủa. - Kim loại nào dưới đây không phản ứng với dung dịch Cu(NO₃)₂?
A. Fe B. Zn C. Ag D. Al
Giải thích: Ag không đẩy được Cu nên không xảy ra phản ứng. - Kim loại nào có thể khử ion Fe³⁺ thành Fe²⁺?
A. Cu B. Zn C. Ag D. Fe
Giải thích: Zn là chất khử mạnh có thể khử Fe³⁺ → Fe²⁺. - Cho Fe dư vào dung dịch chứa hỗn hợp CuSO₄ và ZnSO₄. Kim loại nào thu được?
A. Fe B. Cu C. Zn D. Ag
Giải thích: Fe đẩy Cu ra nhưng không đẩy Zn vì Zn hoạt động mạnh hơn. - Kim loại nào sau đây phản ứng với FeCl₃ tạo ra FeCl₂?
A. Zn B. Cu C. Na D. Al
Giải thích: Cu khử Fe³⁺ → Fe²⁺ tạo muối FeCl₂. - Cho Al vào dung dịch FeCl₃, hiện tượng xảy ra là:
A. Không phản ứng B. Xuất hiện kết tủa Fe C. Có khí thoát ra D. Màu dung dịch không đổi
Giải thích: Al mạnh hơn Fe nên khử ion Fe³⁺ thành Fe kết tủa. - Phản ứng kim loại – muối luôn kèm theo sự:
A. Tỏa nhiệt B. Trao đổi electron C. Hấp thụ nhiệt D. Cắt đứt liên kết ion
Giải thích: Là phản ứng oxi hóa khử nên có sự trao đổi electron. - Phản ứng nào sau đây xảy ra?
A. Cu + ZnCl₂ → B. Zn + FeCl₃ → C. Fe + CuSO₄ → D. Ag + CuSO₄ →
Giải thích: Fe có thể đẩy Cu ra khỏi muối → phản ứng xảy ra. - Kim loại nào sau đây phản ứng với dung dịch Pb(NO₃)₂?
A. Zn B. Cu C. Ag D. Pb
Giải thích: Zn mạnh hơn Pb nên phản ứng xảy ra. - Cho Mg dư vào dung dịch Cu(NO₃)₂ dư. Sau phản ứng thu được chất rắn là:
A. Mg B. Cu C. Ag D. Zn
Giải thích: Mg đẩy Cu ra khỏi dung dịch, Cu là chất rắn thu được.
🔹 Câu Hỏi Đáp
1. Khi nào kim loại không phản ứng với dung dịch muối?
Khi kim loại đó đứng sau kim loại trong muối trong dãy hoạt động hóa học.
2. Dung dịch sau phản ứng có thể chứa những gì?
Muối mới tạo thành, kim loại dư hoặc muối chưa phản ứng.
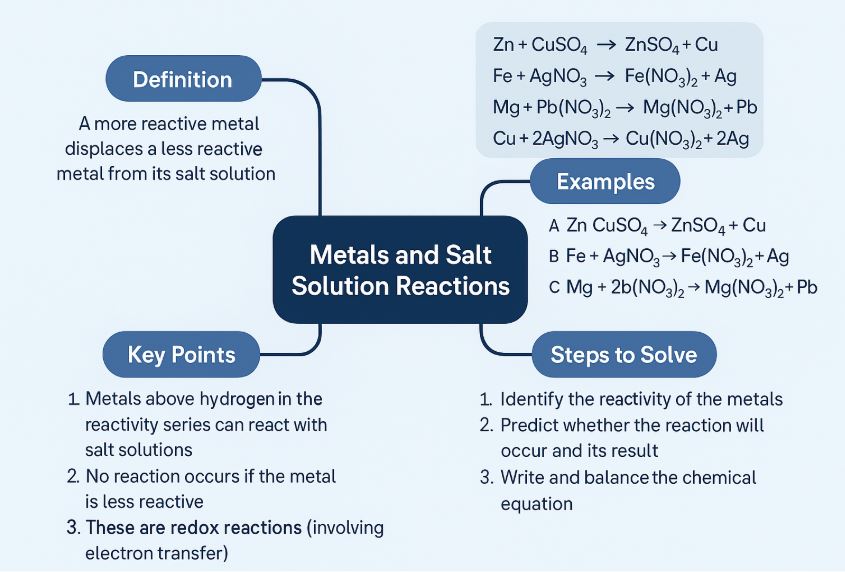
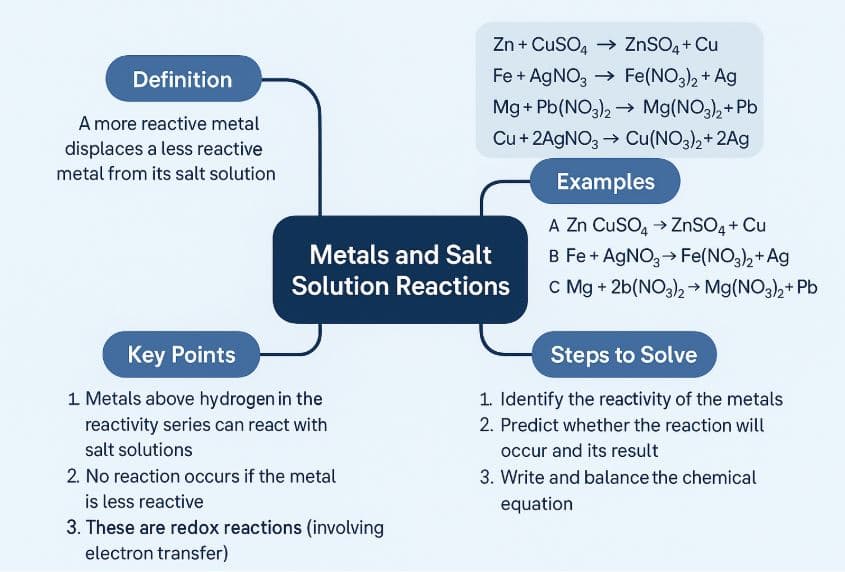
🔹 H. Sơ đồ tư duy minh họa