Bài Tập Về Phương Pháp Tách Kim Loại (Lý Thuyết + Bài Tập)
🔹 A. Lý Thuyết Chung
1. Tách kim loại khỏi hỗn hợp:
Dựa vào tính chất vật lý: khác biệt về nhiệt độ nóng chảy, độ bay hơi, tính dẫn điện…
Dựa vào tính chất hóa học: phản ứng với axit, nước, muối, kiềm…
2. Các phương pháp phổ biến:
Dùng dung dịch axit để hòa tan kim loại hoạt động mạnh.
Điện phân nóng chảy hoặc điện phân dung dịch.
Phản ứng trao đổi trong dung dịch muối.
Lọc, kết tinh, cô cạn – dùng tính tan, điểm sôi khác nhau.
Nhiệt luyện: dùng chất khử (C, CO, Al…) để tách kim loại từ oxit.
🔹 B. Phương Pháp Giải Bài Tập
Bước 1: Xác định hỗn hợp và mục tiêu tách.
Bước 2: Chọn phương pháp thích hợp: hóa học – vật lý.
Bước 3: Viết các phương trình phản ứng.
Bước 4: Tính toán khối lượng, thể tích cần thiết nếu có.
Gợi ý:
Kim loại mạnh có thể đẩy kim loại yếu ra khỏi dung dịch muối.
Dùng dung dịch HCl, H₂SO₄ loãng để hòa tan riêng lẻ kim loại có tính khử mạnh.
🔹 Ví Dụ Minh Họa
Ví dụ 1: Tách Fe khỏi hỗn hợp Fe và Cu.
→ Dùng dung dịch HCl loãng. Fe phản ứng tạo FeCl₂, Cu không phản ứng.
Ví dụ 2: Tách Ag khỏi hỗn hợp Ag và Zn.
→ Dùng dung dịch AgNO₃. Zn phản ứng, Ag không phản ứng → lọc.
Ví dụ 3: Cho hỗn hợp Mg, Al. Tách Al bằng NaOH.
→ Al tan trong NaOH tạo NaAlO₂, Mg không phản ứng. → Lọc → cô cạn NaAlO₂.
🔹 Các Phản Ứng Hóa Học Minh Họa
1. Fe + 2HCl → FeCl₂ + H₂↑
2. Al + NaOH + H₂O → NaAlO₂ + 1.5H₂↑
3. Zn + CuSO₄ → ZnSO₄ + Cu↓
4. AgNO₃ + NaCl → AgCl↓ + NaNO₃
5. Fe₂O₃ + 3CO → 2Fe + 3CO₂
6. 2Al + Fe₂O₃ → 2Fe + Al₂O₃
🔹 Bài Tập Tự Luyện (10 Câu)
- Tách Fe ra khỏi hỗn hợp Fe và Ag?
→ Dùng dung dịch HCl loãng. Fe tan tạo khí H2, Ag không phản ứng. - Hỗn hợp Zn, Cu. Dùng dung dịch nào để tách Cu?
→ Dùng dung dịch HCl loãng: Zn tan, Cu không phản ứng. - Cho Al và Mg. Dùng gì để tách Al?
→ Dùng dung dịch NaOH đặc nóng. Al tan sinh khí H2, Mg không phản ứng. - Cho Fe và Zn. Dùng dung dịch CuSO₄, kim loại nào tan?
→ Cả Zn và Fe đều phản ứng, đẩy Cu ra khỏi muối, Cu kết tủa. - Muối AgNO₃ bị lẫn NaCl. Làm sao tách Ag+?
→ Thêm dung dịch NaCl → tạo kết tủa AgCl → lọc lấy kết tủa → rửa và nhiệt phân nếu cần. - Tách hỗn hợp Mg và Cu bằng hóa học?
→ Cho vào dung dịch HCl: Mg phản ứng, Cu không tan. Lọc lấy Cu. - Tách Pb ra khỏi hỗn hợp Pb và Zn?
→ Dùng dung dịch HCl: Zn tan, Pb không tan. Lọc lấy Pb. - Cho hỗn hợp Fe và FeO, cách tách đơn giản nhất?
→ Dùng từ tính (nam châm): hút Fe ra khỏi FeO (không có tính sắt từ). - Tách hỗn hợp Al₂O₃ và Fe bằng phương pháp vật lý?
→ Dùng nam châm: hút Fe ra khỏi bột oxit Al₂O₃. - Cho hỗn hợp Ba và Fe. Dùng dung dịch nào để tách Fe?
→ Dùng H2O: Ba phản ứng mạnh sinh khí H2, Fe không phản ứng → lọc lấy Fe.
🔹 20 Câu Trắc Nghiệm Tự Chấm
- Kim loại nào sau đây đẩy được Cu ra khỏi dung dịch CuSO₄?
A. Ag B. Au C. Fe D. Hg
→ Fe hoạt động mạnh hơn Cu nên có thể đẩy Cu ra khỏi dung dịch muối. - Cho hỗn hợp Mg và Al vào dung dịch HCl, chất nào phản ứng trước?
A. Mg B. Al C. Cả hai D. Không phản ứng
→ Mg đứng trước Al trong dãy hoạt động hóa học. - Phản ứng nào sau đây là phản ứng trao đổi ion?
A. Fe + HCl → FeCl₂ + H₂ B. AgNO₃ + NaCl → AgCl + NaNO₃ C. Zn + CuSO₄ → ZnSO₄ + Cu D. 2K + H₂O → 2KOH + H₂
→ Phản ứng giữa 2 muối tạo kết tủa là phản ứng trao đổi ion. - Kim loại nào sau đây không phản ứng với dung dịch HCl?
A. Cu B. Mg C. Zn D. Fe
→ Cu đứng sau H trong dãy hoạt động nên không phản ứng với axit. - Thêm Na vào dung dịch CuSO₄, hiện tượng xảy ra là?
A. Na phản ứng với nước, CuSO₄ không phản ứng
→ Na rất hoạt động, phản ứng với nước trước, không phản ứng trực tiếp với CuSO₄. - Cho Fe vào dung dịch AgNO₃, hiện tượng là:
A. Fe tan, Ag kết tủa B. Ag tan C. Có khí thoát ra D. Không phản ứng
→ Fe đẩy Ag ra khỏi muối, tạo kết tủa Ag. - Dung dịch nào có thể hòa tan cả Fe và Zn nhưng không tác dụng với Cu?
A. HCl B. AgNO₃ C. NaCl D. H₂O
→ HCl tan được Fe và Zn, nhưng không tác dụng với Cu. - Al tác dụng với dung dịch NaOH sinh ra khí gì?
A. O₂ B. H₂ C. N₂ D. CO₂
→ Al + NaOH tạo khí H₂ và muối natri aluminat. - Kim loại nào sau đây tác dụng với dung dịch muối tạo ra kim loại khác?
A. Zn + CuSO₄ B. Cu + HCl C. Al + Ag D. Fe + NaCl
→ Zn đẩy Cu ra khỏi muối. - Cho Fe vào dung dịch Cu(NO₃)₂, kim loại tạo thành là?
A. Fe B. Cu C. Al D. Zn
→ Fe đẩy Cu ra khỏi dung dịch. - Kim loại nào sau đây phản ứng được với dung dịch H₂SO₄ loãng và giải phóng khí H₂?
A. Cu B. Zn C. Ag D. Au
→ Zn đứng trước H trong dãy hoạt động nên phản ứng với axit tạo H₂. - Cho mẩu Na vào nước, hiện tượng là:
A. Không phản ứng B. Sôi, khí H₂ thoát ra C. Đổi màu xanh D. Xuất hiện kết tủa
→ Na phản ứng mạnh với nước tạo NaOH và H₂ bay lên, phản ứng tỏa nhiệt. - Phương trình đúng mô tả phản ứng: Mg + HCl →
A. MgCl + H₂ B. MgOH + HCl C. MgCl₂ + H₂ D. Mg₂Cl + H₂O
→ Mg + 2HCl → MgCl₂ + H₂. - Cho Al vào dung dịch FeCl₃, sản phẩm là:
A. Fe và AlCl₃ B. Al và FeCl₂ C. AlCl₃ và khí H₂ D. Không phản ứng
→ Al hoạt động mạnh hơn Fe nên đẩy Fe ra khỏi muối. - Kim loại nào sau đây có thể khử Fe²⁺ về Fe?
A. Mg B. Cu C. Ag D. Pb
→ Mg hoạt động mạnh hơn Fe nên có thể khử Fe²⁺ thành Fe. - Muối nào sau đây không thể bị kim loại Fe khử?
A. NaCl B. AgNO₃ C. CuSO₄ D. Pb(NO₃)₂
→ Fe không đẩy được Na ra khỏi NaCl vì Na đứng trước Fe trong dãy hoạt động. - Phản ứng giữa Zn và CuSO₄ thuộc loại phản ứng:
A. Thế B. Oxi hóa – khử C. Trao đổi D. Nhiệt phân
→ Có sự thay đổi số oxi hóa: Zn → Zn²⁺, Cu²⁺ → Cu. - Kim loại nào có thể phản ứng với dung dịch HCl và nước?
A. Cu B. Na C. Ag D. Au
→ Na là kim loại kiềm phản ứng với cả nước và HCl. - Cho hỗn hợp Al và Cu vào dung dịch H₂SO₄ loãng. Kim loại nào phản ứng?
A. Cu B. Al C. Cả hai D. Không kim loại nào
→ Al đứng trước H nên phản ứng, Cu không phản ứng với axit loãng. - Trong các kim loại sau, kim loại hoạt động mạnh nhất là:
A. K B. Zn C. Fe D. Mg
→ K là kim loại kiềm, đứng đầu dãy hoạt động hóa học.
🔹 5 Câu Hỏi Đáp – Ôn Tập
Câu 1: Làm sao phân biệt hỗn hợp Al và Cu bằng hóa chất?
→ Dùng dung dịch NaOH: Al tan, Cu không tan.
Câu 2: Dùng phương pháp vật lý nào để tách Fe khỏi cát?
→ Dùng nam châm (nam châm hút Fe nhưng không hút cát).
Câu 3: Có thể dùng khí CO tách Fe không?
→ Có. Dùng phương pháp nhiệt luyện: CO khử oxit sắt ở nhiệt độ cao thành Fe tự do.
Câu 4: Vì sao Na được bảo quản trong dầu hỏa?
→ Vì Na phản ứng mãnh liệt với nước và không khí. Dầu hỏa giúp cách ly Na với môi trường ẩm và O2.
Câu 5: Cho Mg, Zn vào dung dịch H2SO4 loãng, chất nào phản ứng mạnh hơn?
→ Mg phản ứng mạnh hơn Zn vì Mg đứng trước Zn trong dãy hoạt động hóa học của kim loại.
🔹 Thông Tin Cần Nhớ
Kim loại mạnh đẩy kim loại yếu khỏi muối.
Một số kim loại phản ứng với axit loãng giải phóng H₂.
Tính tan và độ hoạt động là chìa khóa để chọn phương pháp tách.
Cẩn thận khi dùng NaOH – chỉ kim loại lưỡng tính tan được.
🔹 Sơ Đồ Tư Duy Minh Họa
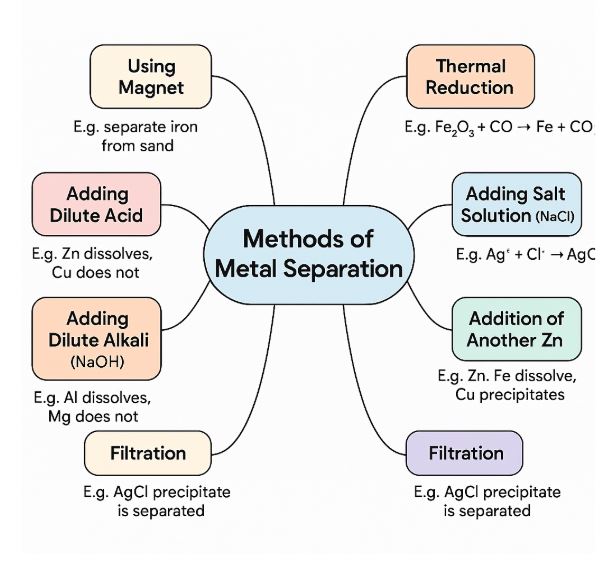
📌 Tải ảnh sơ đồ tư duy tại đây:
👉 Tải sơ đồ tư duy PNG (sẽ cập nhật nếu bạn yêu cầu vẽ)
